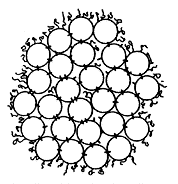
A körök a szubmicellákat,
a vonalak a kalcium-
foszfátot jelzik.
Vázlatos sajtkémia
Koaguláció
A sajtkészítés a tej savanyításával kezdôdik (a laktózt savanyító baktériumtenyészettel alakítják át tejsavvá), majd rendszerint enzimes koagulációval, a kicsapódott alvadék darabolásával és a savó kicsurgatásával folytatódik. Ezt követi a sózás, a formázás és az érlelés.
Az enzimes koaguláció kétlépéses folyamat. Az elsô fázisban a kazeinmicellák destabilizálódnak, a másodikban pedig géllé aggregálódnak.
 |
| Kazeinmicella modellje. A körök a szubmicellákat, a vonalak a kalcium- foszfátot jelzik. |
A tej fehérjéinek mintegy 80%-a kazein, elsôsorban as1-, as1-, b- és k-kazein. A kazein kalcium-foszfáttal 20-300 nm átmérôjû kolloid részecskéket, kazeinmicellákat alkot. Bár a micellák szerkezetét nem ismerik pontosan, általánosan elfogadják, hogy kisebb kazein-aggregátumokból, "szubmicellákból" állnak, és a k-kazein többsége a külsô felületen helyezkedik el. A k-kazein amfipatikus. Az N-terminális a hidrofób a- és b-kazein, illetve a kolloid kalcium-foszfát felé törekszik, ezért inkább a micella belseje felé mutat. A maradék, valószínûleg a molekula nagyobbik része, kinyúlik a felszínbôl, amitôl a micella "szôrös" lesz. A micellák - az oltóenzim nélkül - nem hajlamosak az aggregációra. Ennek feltehetôen az az oka, hogy a hidrofil "szôrök" anionosak, -10 -- -20 mV-os z-potenciált hoznak létre, tehát elektrosztatikusan taszítják egymást, és a "szôrök" sem tudnak egymás közé beférkôzni, így az aggregálódást sztérikus okok is gátolják.
A sajtok oltóanyagát, amelynek a kimozin a legfontosabb enzimje, hagyományosan növendék kérôdzôk, fôként borjak gyomrából nyerik, de proteázokat is használnak a hagyományos oltóanyag pótlására vagy hatásának fokozására.
Az oltóanyag legfontosabb szerepe az, hogy a k-kazeint a fehérje Phe105-Met106-os kötésénél hidrolizálja. Az elsôdleges szerkezet és a környezô aminosavak konformációja miatt ez a kötés az összes többi peptidkötésnél hajlamosabb a savas hidrolízísre, amelynek hatására a micellák "szôreinek" többsége távozik, és a z-potenciál -5 -- -7 mV közé kerül. Így a micellák közötti elektrosztatikus taszítás és sztérikus gátlás csökken, a micellák destabilizálódnak.
A k-kazein hidrolízisét befolyásolja az oltóanyag és a Ca2+-ion koncentrációja, az ionerôsség, a hômérséklet és a pH. Az optimális pH 5,0-5,5, de a kimozin az "édes" tej 6,6-6,8-as pH-ján is megindítja a kicsapódást.
A koaguláció második szakaszában aggregáció játszódik le. A micellák elôször láncokat képeznek, majd kialakul a gélekre jellemzô hálós szerkezet, amely a zsírcseppeket is magába zárja. A folyamatban fontos szerepet játszanak a Ca2+-ionok; az ionok valószínûleg a térhálósodást segítik elô vagy a micellák felületi töltéseit semlegesítik. Az aggregálódás hômérsékletfüggô; 15 oC alatt nem játszódik le (a kazeint általában 31 oC körüli hômérsékleten koaguláltatják). Ha a gélképzôdés kellôképpen elôrehaladt, az alvadékot feldarabolják, hogy a savó kiszivároghasson.
Sajtérlelés
Az oltóanyaggal koaguláltatott sajtok többségét legalább négy hétig érlelik fogyasztás elôtt. Az érlelés során számos biokémiai folyamat zajlik le, és ekkor alakul ki az egyes fajtákra jellemzô íz és textúra.
Az érleléskor lejátszódó legfontosabb biokémiai változás a laktóz/laktát átalakulás, a proteolízis és a lipolízis. A folyamatokat az oltóanyag maradéka, a baktériumtenyészet enizmei, a tej saját enzimei és a tejhez vagy a sajthoz adott enzimek váltják ki.
A sajtban levô mikroorganizmusok fô energiaforrása a laktóz. A friss (egynapos) sajtban a laktóz koncentrációja < 0,1%-tól (holland és ementáli típusú sajtok) körülbelül 1%-ig változik (cheddar). A maradék laktózból a baktériumok hatására L(+)- és D(-)-laktát keletkezik.
Az L(+)-laktátot a propionsav-bakétriumok propionsavvá, ecetsavvá és szén-dioxiddá alakítják át az ementáli típusú sajtokban.
| 3CH3CHOHCOOH | --> | 2 CH3CH2COOH + | CH3COOH + CO2 + H2O |
| tejsav | propionsav | ecetsav |
A szén-dioxid egy része felhalmozódik a sajtban, és kialakulnak a jellegzetes lyukak.
A laktát-átalakulás és a proteolíziskor keletkezô lúgos nitrogénvegyületek hatására az érés során a legtöbb sajféleség pH-ja nô. Hat hónap után az ementáli típusú sajtok pH-ja 5,3-ról kb. 5,9-re, a camembert és a kék sajtok pH-ja 4,8-ról kb. 7-re emelkedik.
A sajtban levô fehérjék egy része a maradék oltóanyag és egyéb enzimek hatására polipeptidekre, majd az íz szempontjából fontos kisebb peptidekre és aminosavakra bomlik le. A sajtban a következô szabad aminosavak fordulnak elô a leggyakrabban: glutaminsav, metionin, aszparagin, hisztidin, alanin, valin, fenil-alanin, leucin és lizin. Az ementáli típusú sajtokban prolin is van.
A lipáz a triglicerideket zsírsavakká, mono- és digliceridekké alakítja át. A baktériumtenyészetek olyan lipázokat tartalmaznak, amelyek a mono- és diglicerideket hidrolizálják. Ezért a szabad (C4-C18) zsírsavak koncentrációja a baktériumokkal érlelt sajtokban, például a cheddarban, az ementáli és a holland típusú sajtokban kicsi. A kék sajtokban és néhány olasz sajtban, például a parmezánban, háromszor annyi zsírsav van, mint a cheddarban.
A sajt érése során a zsír a következô lépésekben bomlik le: a lipáz hatására zsírsavak, mono- és digliceridek keletkeznek, a zsírsavak b-keto-savakká oxidálódnak, a b-keto-savak dekarboxilezôdésével metil-ketonok keletkeznek, amelyek szekunder alkoholokká bomlanak el.
A rövid láncú (C4-C10) zsírsavak, a metil-ketonok (fôként a 2-heptanon, kisebb mértékben a 2-nonanon és a 2-pentanon), valamint a szekunder alkoholok a sajtok jellegzetes ízében éreztetik hatásukat.
Irodalom:
Encyclopaedia of Food Science, Food Technology and Nutrition, Vol. 2, Academic
Press, London,1993
Römpp Vegyészeti Lexikon, 4. kötet, Mûszaki Könyvkiadó,
Budapest, 1984
Britannica Hungarica, 6. kötet, Magyar Világ Kiadó,
Budapest, 1997