Johann Wilhelm Hittorf
(18241914)
Az ionok elektrolízis közbeni vándorlásáról
Részletek
Annalen der Physisik und Chemie, 89: 177211 (1853), 98: 133 (1856), 103: 156 (1858), 106: 337411, 513586 (1859)
in: Henry Marshall Leicester and Herbert S. Klickstein, A Source
Book in Chemistry 14001900 (Harvard University Press, Cambridge, Massachusetts,
1963)
 |
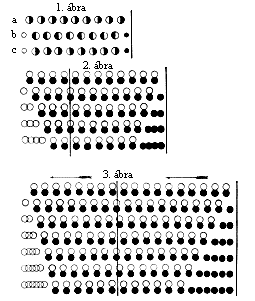
| Hittorf ábrája az iontranszporthoz |
Az áram hatására az elbontandó test részecskéi elõször olyan helyzetbe kerülnek, hogy minden molekula kationja a katód felé, anionja az anód felé fordul. A két ion ezután elválik egymástól, ellentétes irányba mozdul el, és találkozik a hasonlóképpen vándorló, szomszédos ionokkal (1.b ábra). A folyamat révén azonban olyan helyzetbe jutnak, amikor minden anion a katód, és minden kation az anód felé fordul. Ezért minden molekulának el kell fordulnia, és ellentétes helyzetet kell felvennie, hogy ugyanannál az elektródnál ugyanaz a komponens szabadulhasson fel folyamatosan (1.c ábra).
Igen fontos lenne, ha azokat a mozgásokat, amelyeknek az áram áthaladása során az elektrolit legkisebb részecskéi is ki vannak téve, az általános képnél pontosabban írhatnánk le. Ekkor az elektromosságon kívül a testek kémiai felépítésének természetére is felvilágosítást nyernénk.
Sok esetben kísérlettel meghatározhatók azok a relatív távolságok, amelyeket a két ion az elektrolízis során megtesz. Mivel a következõkben csak ennek szenteljük figyelmünket, egyedül ezt emeljük ki az ábrán. Ebbõl a célból alkalmazzuk Berzelius ábrázolásmódját, amely a két iont egymás alatt tünteti fel, és feltételezi, hogy az ionok vízszintes irányban mozdulnak el (2. ábra). Azt is feltesszük, hogy az elektrolitot közömbös, nem vezetõ oldószer hozta folyékony állapotba.
Ha az oldatot egy adott helyen elvágnánk, azt találnánk, hogy az ionok aránya a vágás mentén mindenhol megváltozik az elektrolízis hatására. Ezt az arányt az a távolság határozza meg, amelyet az egyes ionok az áram áthaladása folyamán megtesznek.
Ha például a korábbi ábrázolásoknak azzal a hallgatólagos feltevésével élünk, hogy ezek a távolságok egyenlõk, mely esetben a két vándorló ion az eredeti helyzetük közötti félúton találkozik, a 2. ábrából azonnal kitûnik, hogy az elektrolízis után az anóddal határos folyadékrész fél egyenértéknyivel kevesebb kationt tartalmaz, mint korábban. Természetesen ennek ellenkezõje áll fenn a katóddal érintkezõ részre. Egyenérték alatt a felszabadított komponens mennyiségét értjük.
Ha a két ion nem azonos távolságot tesz meg tehát nem találkozik félúton , a folyadéknak azon része, amelyben a gyorsabban mozgó ion megjelenik, fél egyenértéknyinél többet tartalmaz majd ebbõl az ionból, míg a másik ion mennyisége fél egyenértéknyinél kevesebbel csökken benne. A 3. ábra olyan estetet reprezentál, amikor az anion a távolság 1/3, a kation a távolság 2/3 részét teszi meg, A folyadék anód felõli oldala 1/3 egyenértéknyivel több aniont, és 2/3 egyentértéknyivel kevesebb kationt tartalmaz a bomlás után, mint elõtte. A másik oldal az ellenkezõ arányt mutatja.
Az eredmény nyilvánvalóan általánosan érvényes. Ha az egyik ion a távolság 1/n-ed részét teszi meg, és a másik az (n1)/n-ed részét, akkor a folyadéknak az a része, amelyikben az elõzõ ion megjelenik, 1/n egyenértéknyivel többet tartalmaz majd belõle, míg a másikból (n1)/n egyenértéknyivel kevesebbet tartalmaz. Az elektrolit másik felében az ellenkezõ arány érvényesül.
[Hittorf kísérleti eredményeit ismerteti a következõ idézetben.]
1. Úgy tûnik, hogy azok a kémiai események, amelyek révén az elektrolitok átadják az elektromos áramot, csak abban a két rétegben játszódnak le, amelyek közvetlenül érintkeznek az elektródokkal; az elektrolízis feltehetõen nem változtatja meg a többi réteget. Ez nemcsak akkor áll fenn, ha az elektrolit hõ hatására cseppfolyósodik; maga az oldat is hasonló módon viselkedik. Ha megakadályozzuk, hogy ezek a határrétegek keveredjenek a közöttük levõvel, ez utóbbi megtartja eredeti koncentrációját, amíg az áram átfolyik rajta. Az olvadt elektrolitokban az elektrolízis bomlástermékeinek tanulmányozása korlátozott; a bomlástermékeknek az áramerõsséggel, valamint az elektrolitok természetével való kapcsolatát Faraday klasszikus munkája tárgyalja. Az elektrolitok oldatában még egy eleddig igen kevéssé ismert jelenség érvényesül. A határrétegekben, amelyekben az ionok szabadok, megváltozik az ionok koncentrációja.
2. A jelenséget az elektropozitív fémek sói mutatják a legjobban. Ezeket a sókat az oldószerek nem bontják szét, ezért ezekkel foglalkozunk elõször. Ezekben a sóoldatokban az a réteg, amelyikben a fém felszabadul, felhígul, miközben az elektronegatív rész különválását koncentrációnövekedés kíséri, ha gondoskodunk róla, hogy az anód oldható vegyületet képezzen vele. Az utóbbi feltétel igen jól teljesíthetõ, ha ugyanazt a fémet választjuk anódnak, mint amelyiknek a sóit tesszük ki az áram hatásának. A legjobban akkor látjuk ezt a folyamatot, ha a katódot az edény fölsõ részén, az anódot pedig lejjebb helyezzük el. Ekkor kitûnik, hogy az elektródokkal nem érintkezõ folyadékrétegek hogyan tartják meg eredeti sûrûségüket.
3. Ezeknek a jelenségek a jobb megértése érdekében kavantitatíve meg kell határoznunk a hígulás és a koncentrációnövekedés mértékét. Az itt tárgyalt viselkedés automatikusan következik a fentiekbõl. Egy oldatot, amelynek függõlegesen minden rétegében ismerjük a koncentrációját, áram hatásának teszünk ki, az elektrolízis után a két elektród között bárhol szétválasztjuk, amíg nem keveredik a határrétegekkel, és végül meghatározzuk annak a folyadéknak az összetételét, amelyik a két rész egyikében van. Elméletileg nem jelent különbséget, hogy melyiket választjuk, mert a két rész együtt az eredeti oldatot alkotja. [...]
5. A vizsgálat megadja az adott súlyú oldatban levõ bármely ion mennyiségét, ha az áram hatására adott mennyiségû só bomlik el. Mivel a változatlan oldat tartalma ismert, tudjuk, hogy az elektrolízis elõtt mekkora tömegû ion található tetszõleges súlyú oldószerben, és a különbség megadja azoknak az ionoknak a súlyát, amelyeket az áram szállított a kérdéses pólushoz vagy amelyek szétváltak az áram hatására. Ezek a különbségek azonban arányosak az áram által elbontott mennyiségekkel. A jelenség minden hipotézistõl függetlennek tûnik.
[A következõ részbõl kiderul, hogy Hittorf milyen közel jutott az elektrolitos disszociáció elméletéhez.]
Clausius nemrégiben adott magyarázatot az elektrolitok vezetésére az elektromosság elméletének fogalmai alapján, és ennek során figyelembe vette a transzportjelenségeket. Feltevése szerint az elektromos erõt az elektromos fluidum hordozza, melynek ponderábilis atomjai elválaszthatatlanok egymástól, és ennek megfelelõen az elektrolízis folytonos folyamat, melynek az elektrolitok felületén található szabad elektromosság szab határt. A Clausius feltevései alapján levont következtetés vitathatatlan. A Faraday-törvény, amely igen gyenge áramra is érvényes, ellentétben áll a modern kémiával a folyékony, összetett test állapotát illetõen. Az elektrolitok ionjai nem állhatnak össze stabil módon teljes molekulákká, és ezek nem létezhetnek határozott, szabályos elrendezésben.
[A következõ részben Hittorf az oldatok viselkedését a gázokéhoz hasonlítja.]
A koncentrált kadmium-jodid-oldatok vizsgálatakor kapott eredmények jelentõsen eltérnek a korábban kapottaktól. Elektrolízis után mindkét komponens mennyisége nõ az anódnál, s mivel a középsõ réteg megtartja az összetételét, ugyanekkora csökkenés jelentkezik a katódnál.
Az elõzõhöz hasonló magyarázat alapján a jód- és a kadmiumionok úgy mozdulnak el az anód felé, hogy az elsõ mindig nagyobb távolságot tesz meg, mit két sómolekula távolsága, és megelõzi a fémet, amely ebben az esetben nagyon lassan vándorol. Az I. oldatban például a jód minden szétváláskor és újraegyesüléskor a két sómolekula távolságának kb. egy és egynegyedével, a kadmium kb. egyötödével közelíti meg az anódot. Ezt a magyarázatot nyilvánvalóan el kell vetni, és újabbat kell keresni.
A kettõs sóban (ICd+IK) a kadmium az összes jóddal az anód felé halad; a kadmium-jodid híg oldatában a kadmium a fémek szokásos viselkedését követi, a katód felé mozdul el, s a két sómolekula távolságának kb. kétötödét, a jód a háromötödét teszi meg.
Sok vegyész manapság feltételezi, hogy számos elemi és összetett gázban az atomok kettesével egyesülnek, más szóval azonos szubsztanciák között tételeznek fel vegyülést, amit a régi iskola abszurdumnak tekintett. Annak, aki elég sokat foglalkozik az oldatok tulajdonságaival, önkéntelenül rá kell jönnie az oldott testek és a gáznemû testek közötti analógiára.
A fenti eredmények arra a feltevésre késztetnek, hogy a koncentrált oldatokban kettõs sók vannak, melyek két egyenérték ICd-t tartalmaznak és az árammal szemben úgy viselkednek, mintha két különbözõ fémbõl állnának. Elektrolízis során (ICd+I)-re és Cd-re válnak szét. A kadmium fele a katód felé vándorol, míg másik fele az összes jóddal az anódhoz megy. ...
Az átviteli szám és az oldat koncentrációjának fontos összefüggése ugyanúgy magyarázható, mint a kettõs sók (ICd+IK) esetén. Víz hozzáadásakor a kettõs atomok egyre nagyobb számban bomlanak fel egyszerû atomokká, ezért az áramot egyre inkább az egyszerû atomok vezetik, amelyek erõs hígításban vannak csak önmagukban jelen.
[A következõ részben Hittorf az elektrolitok kémiai tulajdonságáról fejti ki nézetét.]
Az új kémia értelmében minden elektrolit só. Az elektrolízis folyamán ugyanolyan csere játszódik le molekuláik komponensei között, mint cserebomláskor. Ugyanez a jelenség idézi elõ azt a molekuláris mozgást, amelyet elektromos áramnak nevezünk. Annak megfelelõen, hogy ez a csere a különbözõ elektrolitokban gyorsabban vagy lassabban megy végbe ugyanazon kiváltó ok hatására, véleményem szerint különbözõ ellenállásokat eredményez. Remélem, hogy elektrokémiai munkám kiegészítéseként ellenállásmérések sorával támaszthatom alá ezt az összefüggést. Ezek a különbségek akkor nyilvánulnak meg a kémiai jelenségekben, ha különlegesen nagyok.
| Vissza | http://www.kfki.hu/chemonet/
http://www.ch.bme.hu/chemonet/ |