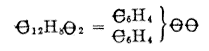Friedrich August Kekulé
(18291896)
Vizsgálatok az aromás vegyületek
körében
Részletek
Annalen der Chemie, 137: 129196 (1865)
in: Henry Marshall Leicester and Herbert S. Klickstein, A Source
Book in Chemistry 1400-1900 (Harvard University Press,
Cambridge, Massachusetts, 1963)
 Az elemek
atomicitásának elmélete, és elsõsorban
a szén tetratomos elemkénti+
felfogása az utóbbi években igen alkalmas módot
kínált számos szénvegyület atomi konstitúciójának
magyarázatára, legfõképpen azokéra,
amelyeket zsíros testeknek nevezek. Tudomásom szerint
eleddig senki sem kísérelte meg, hogy ezeket az elgondolásokat
az aromás vegyületekre is kiterjessze. Hét évvel
ezelõtt, amikor a szén tetratomos természetére
vonatkozó nézeteimet kifejtettem, már jeleztem, hogy
errõl is van elképzelésem, de akkor nem tartottam
idõszerûnek a probléma tüzetesebb vizsgálatát.
Azoknak a kémikusoknak a többsége, akik azóta
elméleti kérdéseket fejtegettek, nem érintette
a kérdést; néhányan határozottan kijelentették,
hogy az aromás vegyületek összetétele nem magyarázható
meg az atomicitás elméletével, mások hat szénatomból
álló hatatomos csoportot tételeztek fel, de sem arra
nem tettek kísérletet, hogy megtalálják a szénatomok
kapcsolódási módját, sem arra, hogy megtalálják
a hat monatomos elem csoporttá alakulásának feltételeit.
Az elemek
atomicitásának elmélete, és elsõsorban
a szén tetratomos elemkénti+
felfogása az utóbbi években igen alkalmas módot
kínált számos szénvegyület atomi konstitúciójának
magyarázatára, legfõképpen azokéra,
amelyeket zsíros testeknek nevezek. Tudomásom szerint
eleddig senki sem kísérelte meg, hogy ezeket az elgondolásokat
az aromás vegyületekre is kiterjessze. Hét évvel
ezelõtt, amikor a szén tetratomos természetére
vonatkozó nézeteimet kifejtettem, már jeleztem, hogy
errõl is van elképzelésem, de akkor nem tartottam
idõszerûnek a probléma tüzetesebb vizsgálatát.
Azoknak a kémikusoknak a többsége, akik azóta
elméleti kérdéseket fejtegettek, nem érintette
a kérdést; néhányan határozottan kijelentették,
hogy az aromás vegyületek összetétele nem magyarázható
meg az atomicitás elméletével, mások hat szénatomból
álló hatatomos csoportot tételeztek fel, de sem arra
nem tettek kísérletet, hogy megtalálják a szénatomok
kapcsolódási módját, sem arra, hogy megtalálják
a hat monatomos elem csoporttá alakulásának feltételeit.
Az aromás vegyületek atomi konstitúciójának
leírásához figyelembe kell vennünk az alábbi
jelenségeket:
1. Minden aromás vegyület, még a legegyszerûbb
is, gazdagabb szénben, mint a zsíros testek osztályába
tartozó analóg vegyület.
2. Az aromás vegyületek között, a zsíros
testekhez hasonlóan, számos homológ anyag van; ezek
összetételének különbsége n 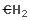 -vel
fejezhetõ ki.
-vel
fejezhetõ ki.
3. A legegyszerûbb aromás vegyület legalább
hat szénatomot tartalmaz.
4. Az aromás anyagok minden módosított terméke
bizonyos hasonlóságot mutat, mindannyian az "aromás
vegyületek" családjába tartoznak. Igaz ugyan, hogy erõsebb
hatású reakciókban a szén egy része
gyakran eltávozik, de a fõ termék legalább
hat szénatomot tartalmaz (benzol, kinon, klóranil, karbolsav,
hidroxi-karbolsav, pikrinsav stb.) Ezeknél a termékeknék
a bomlás leáll, ha a szerves vegyület nem roncsolódik
teljesen szét.
A fenti jelenségek nyilvánvalóan ahhoz a következtetéshez
vezetnek, hogy az összes aromás vegyületben egyazon atomcsoport,
vagy, ha jobban tetszik, ugyanaz a hat szénatomos mag található.
Ebben a magban a szénatomok biztosan erõsen összetartoznak
vagy a többinél kompaktabban vannak elrendezve. Ehhez a maghoz
több szénatom is csatlakozhat ugyanúgy és ugyanolyan
törvények szerint, mint a zsíros testek esetében.
Ezután ennek a magnak az atomi konstitúciójáról
kell számot adnunk. Ez igen könnyû a következõ
hipotézissel, amely a szén tetratomosságának
már általánosan elfogadott felfogása alapján
oly egyszerû magyarázatot ad, hogy további fejtegetésre
aligha van szükség.
Ha sok szénatom képes egymással egyesülni,
megtörténhet, hogy az egyik atom egyetlen affinitásegysége
a szomszédos atom egyetlen affinitásegységéhez
kötõdik. Amint korábban kimutattam, ez magyarázatot
ad a zsíros testek homológiájára és
általában a konstitúciójukra.
Feltételezhetõ továbbá, hogy sok szénatom
ily módon kapcsolódik össze, de vannak olyanok is, amelyek
két affinitásegységgel kötõdnek egymáshoz,
és az is elképzelhetõ, hogy az egyesülés
váltakozva jön létre egy és két
affinitásegységgel. Az elsõ és az utolsó
eset a következõ sorozatokkal jellemezhetõ:
1/1, 1/1, 1/1, 1/1 stb.
1/1, 1/2, 1/1, 1/2 stb.
Amint említettük, a szénatomok egyesülésének
szimmetriájára vonatkozó elsõ törvény
megmagyrázza a zsíros testek konstitúcióját;
a második az aromás vegyületek vagy legalábbis
az összes ilyen vegyületben közös mag konstítúciójának
magyarázatához vezet.
Ha elfogadjuk, hogy hat szénatom kapcsolódik össze
eszerint a szimmetriatörvény szerint, olyan csoportot kapunk,
amelyet ha nyitott láncúnak tekintünk, nyolc
telítetlen affinitásegységet tartalmaz (II. táblázat,
1. ábra). Ha egy másik feltevéssel élünk,
mely szerint a lánc végén a két szénatom
egy affintásegységgel kapcsolódik össze, akkor
zárt láncot* (szimmetrikus gyûrût)
kapunk, s ebben még hat szabad affinitásegység
van (II. táblázat, 2. ábra).**
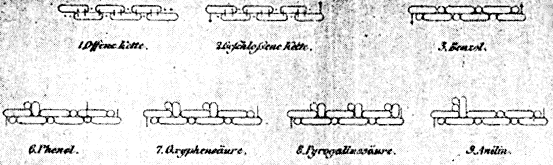
Részlet Kekulé táblázatából
Mármost ebbõl a zárt láncból
következik az összes olyan anyag, amelyet rendszerint aromás
vegyületnek nevezünk. A nyílt lánc a kinonban,
a klóranilban és a mindkettõvel közeli rokonságban
álló néhány vegyületben jelenik meg. Ezekkel
a testekkel nem foglalkozunk tovább; magyarázatok egyszerû.
Látható, hogy szoros rokonságban állnak az
aromás anyagokkal, de nem sorolhatók közéjük.
Feltételezhetõ, hogy minden aromás anyagban van
egy közös mag; ez a zárt lánc, 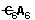 (ahol
A telítetlen affinitás vagy affinitásegység).
(ahol
A telítetlen affinitás vagy affinitásegység).
Eme mag hat affinitásegysége hat monatomos elemmel telíthetõ.
Az affinitásegységek, legalábbis részben, poliatomos
elem egyik egyik affinitásával is telíthetõk,
de az elemnek más atomokhoz is kell kapcsolódnia, ezért
egy vagy több oldallánc keletkezik, amely más
atomokhoz kapcsolódva tovább növekedhet.
A mag két affinitásegységének telítése
diatomos elem atomjával vagy három affinitásegységének
telítése triatomos elem atomjával elméletileg
nem lehetséges. Így a 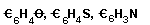 képletû
vegyületek elképzelhetetlenek; ha ilyen össztételû
testek léteznek, és ha az elmélet helyes, az elsõ
kettõ képleteit meg kell kettõzni, a harmadikét
meg kell háromszorozni.***
képletû
vegyületek elképzelhetetlenek; ha ilyen össztételû
testek léteznek, és ha az elmélet helyes, az elsõ
kettõ képleteit meg kell kettõzni, a harmadikét
meg kell háromszorozni.***
+ Kekulé hosszas gondolkodás
után döntötte el, hogy a régi egyenértékeket
(és C=6-ot) vagy azokat a relatív atomtömegeket (C=12)
használja-e, amelyeket Gerhardt javasolt 1843-ban. Az utóbbiak
mellett döntött, és átvette Berzelius jelölését
is, az áthúzott vegyjeleket. Kekulétõl származik
az "affinitásegységek" mai szóval vegyértékkötések
fogalma. Õ ismerte fel, hogy a szén "tetratomos" elem.
Ennek alapján tudta rendszerezni az alifás vegyületeket.
Elméletének egyik fontos következménye volt,
hogy a szénatomok összekapcsolódhatnak egymással.
Az aromás vegyületekrõl Kekulé 1858-ban még
csak annyit állított, hogy "sûrûbb" elrendezésûek
az alifásoknál. Itt idézett híres dolgozata,
amelyben a benzolt gyûrûs vegyületként írja
le, 1865-ben jelent meg
* A zsíros testek csoportjában az etilénsor
szénhidrogénjei zárt láncúaknak tekinthetõk.
Világosan kell látni, hogy az etilén ennek a sornak
kezdõ tagja, és a 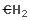 (metilén)
szénhidrogén nem létezik, mert nem hihetõ,
hogy ugyanahhoz a szénatomhoz tartozó két affinitás
képes legyen egymáshoz kapcsolódni.
(metilén)
szénhidrogén nem létezik, mert nem hihetõ,
hogy ugyanahhoz a szénatomhoz tartozó két affinitás
képes legyen egymáshoz kapcsolódni.
** Hogy az itt kifejtett elgondolásokat jobban
megvilágítsam, a II. táblázatban számos
vegyület "grafikus képletét" is összegyûjtöttem.
A képletekkel szemléltetett elképzelések ma
már olyannyira ismertek, hogy szükségtelen részletesen
tárgyalnom õket. Ugyanolyan típusú grafikus
képleteket használtam, mint 1859-ben, amikor elõször
fejleszettem tovább a molekulák atomi konstitúciójára
vonatkozó elgondolásaimat. Ezt a formát említésre
méltó módosítás nélkül fogadta
el Wurtz (Leçons de philosophie chimique), és úgy
vélem, bizonyos elõnyökkel jár a Loschmidt- és
Crum-Brown-féle mostani módosításokkal szemben.
A táblázat mégértéséhez csak
annyit kell megjegyeznem, hogy a 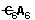 zárt
láncot egyenes vonallal, tehát nyitva jelöltem, a rövid
vonalakkal a szélsõ helyzetben levõ affinitásokat
jelöltem, amelyeket az ellentétes végekhez kötõdõ
affinitásegységekként kell értelmezni. Az 1.,
2., 31. és 32. képleteken a pontok még telítetlen
affinitásegységeket jelentenek.
zárt
láncot egyenes vonallal, tehát nyitva jelöltem, a rövid
vonalakkal a szélsõ helyzetben levõ affinitásokat
jelöltem, amelyeket az ellentétes végekhez kötõdõ
affinitásegységekként kell értelmezni. Az 1.,
2., 31. és 32. képleteken a pontok még telítetlen
affinitásegységeket jelentenek.
*** Emlékszem azonban a 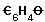 vegyületre, amelyet Limpricht kapott a fenol mellett a szalicilsavanhidrid
száraz desztillációjakor. Ennek az anyagnak a képlete
nyilvánvalóan
vegyületre, amelyet Limpricht kapott a fenol mellett a szalicilsavanhidrid
száraz desztillációjakor. Ennek az anyagnak a képlete
nyilvánvalóan
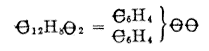 Képzõdését a következõ egyenlet
írja le:
Képzõdését a következõ egyenlet
írja le:
| Vissza |
http://www.kfki.hu/chemonet/
http://www.ch.bme.hu/chemonet/ |
 Az elemek
atomicitásának elmélete, és elsõsorban
a szén tetratomos elemkénti+
felfogása az utóbbi években igen alkalmas módot
kínált számos szénvegyület atomi konstitúciójának
magyarázatára, legfõképpen azokéra,
amelyeket zsíros testeknek nevezek. Tudomásom szerint
eleddig senki sem kísérelte meg, hogy ezeket az elgondolásokat
az aromás vegyületekre is kiterjessze. Hét évvel
ezelõtt, amikor a szén tetratomos természetére
vonatkozó nézeteimet kifejtettem, már jeleztem, hogy
errõl is van elképzelésem, de akkor nem tartottam
idõszerûnek a probléma tüzetesebb vizsgálatát.
Azoknak a kémikusoknak a többsége, akik azóta
elméleti kérdéseket fejtegettek, nem érintette
a kérdést; néhányan határozottan kijelentették,
hogy az aromás vegyületek összetétele nem magyarázható
meg az atomicitás elméletével, mások hat szénatomból
álló hatatomos csoportot tételeztek fel, de sem arra
nem tettek kísérletet, hogy megtalálják a szénatomok
kapcsolódási módját, sem arra, hogy megtalálják
a hat monatomos elem csoporttá alakulásának feltételeit.
Az elemek
atomicitásának elmélete, és elsõsorban
a szén tetratomos elemkénti+
felfogása az utóbbi években igen alkalmas módot
kínált számos szénvegyület atomi konstitúciójának
magyarázatára, legfõképpen azokéra,
amelyeket zsíros testeknek nevezek. Tudomásom szerint
eleddig senki sem kísérelte meg, hogy ezeket az elgondolásokat
az aromás vegyületekre is kiterjessze. Hét évvel
ezelõtt, amikor a szén tetratomos természetére
vonatkozó nézeteimet kifejtettem, már jeleztem, hogy
errõl is van elképzelésem, de akkor nem tartottam
idõszerûnek a probléma tüzetesebb vizsgálatát.
Azoknak a kémikusoknak a többsége, akik azóta
elméleti kérdéseket fejtegettek, nem érintette
a kérdést; néhányan határozottan kijelentették,
hogy az aromás vegyületek összetétele nem magyarázható
meg az atomicitás elméletével, mások hat szénatomból
álló hatatomos csoportot tételeztek fel, de sem arra
nem tettek kísérletet, hogy megtalálják a szénatomok
kapcsolódási módját, sem arra, hogy megtalálják
a hat monatomos elem csoporttá alakulásának feltételeit.