a)
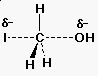
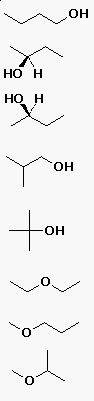 |
1-butanol |
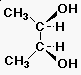
| (S)-2-butanol | |
| (R)-2-butanol | |
| 2-metil-1-propanol (izobutil-alkohol) |
|
| 2-metil-2-propanol (terc-butil-alkohol) |
|
| dietil-éter | |
| metil-propil-éter | |
| metil-izopropil-éter |
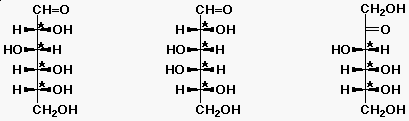 |
||
| D-glükóz | D-galaktóz | D-fruktóz |
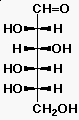

| a) | addíció | |
| b) | 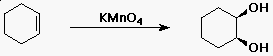 |
addíció (vagy oxidáció) |
| c) | 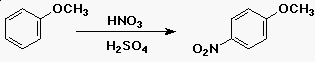 |
szubsztitúció |
| d) | 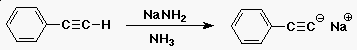 |
sav/bázis |
| e) | 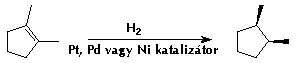 |
addíció (vagy redukció) |
| f) | 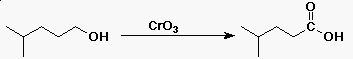 |
oxidáció |
| g) | 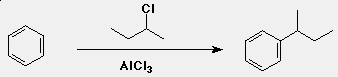 |
szubsztitúció |
| h) | 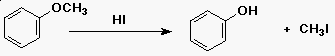 |
szubsztitúció |
| i) |  |
szubsztitúció |
| j) | 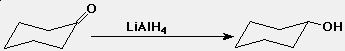 |
redukció (vagy addíció) |

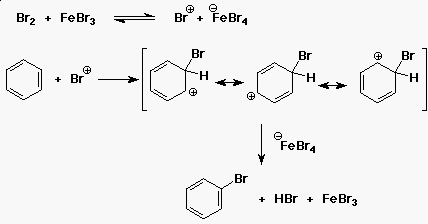
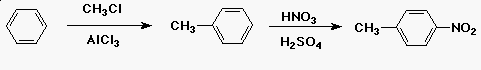 |
| (és némi orto) |